 シルミー
シルミーはかせ、3人に1人の脳に寄生虫がいるって聞いたんだけど、怖くない?
トキソプラズマという寄生虫のことですね。確かに多くの人が感染していますが、実はほとんど発症しないんです。バージニア大学の研究チームが、その仕組みを解明したんですよ
世界中で約30%の人が感染しているとされるトキソプラズマ・ゴンディ。この寄生虫は猫を最終宿主とし、人間の脳にも侵入する。だが驚くべきことに、健康な人はほぼ無症状だ。
バージニア大学の研究チームは、この謎を解く鍵を発見した。感染した免疫細胞には「自爆スイッチ」が組み込まれており、寄生虫ごと自壊するメカニズムが働いていたのだ。
トキソプラズマの驚異的な生存戦略
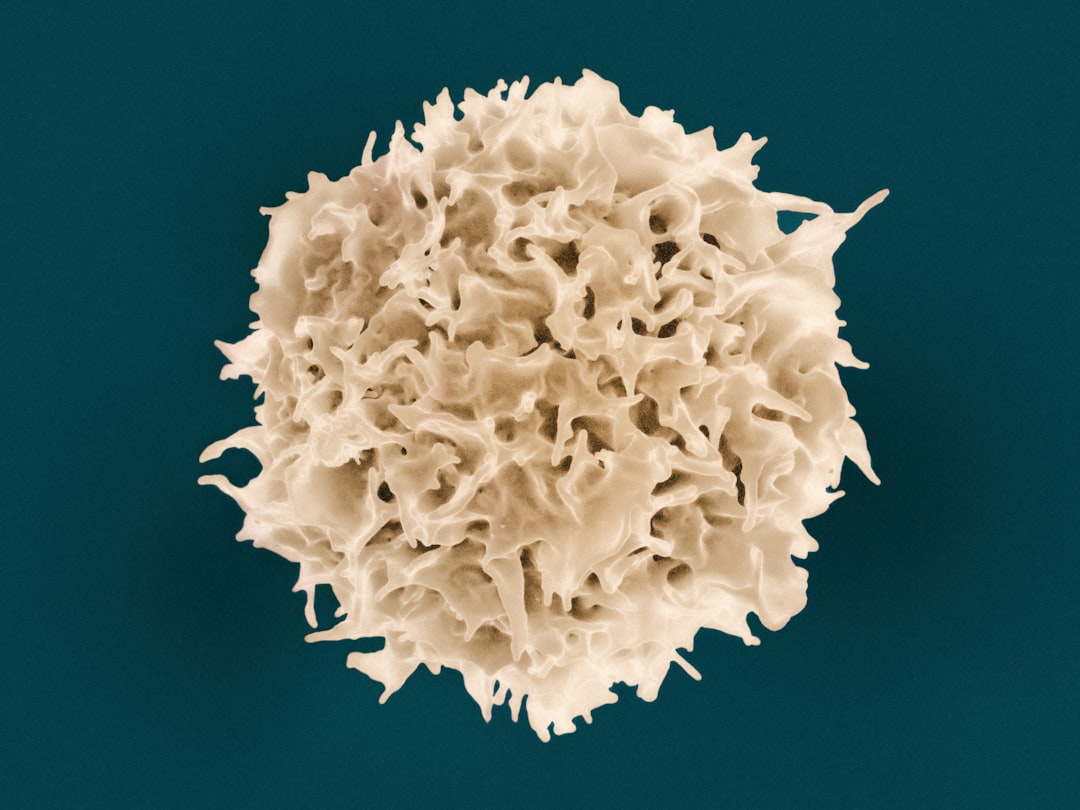

免疫細胞に侵入する狡猾な手口
トキソプラズマ・ゴンディは、単細胞の寄生性原虫だ。体長わずか数マイクロメートルのこの生物は、哺乳類や鳥類など温血動物に広く感染する。
猫の糞便中に排出されたオーシスト(卵のような構造体)が、野菜や土、水を介して人間の口に入る。胃腸で孵化した寄生虫は、血流に乗って全身に広がり、最終的に脳や筋肉に到達する。
ここからが驚異的だ。体内に侵入した寄生虫を撃退するため、免疫システムはCD8+T細胞という特殊部隊を派遣する。ところがトキソプラズマは、この攻撃部隊そのものに侵入してしまう。
まるでトロイの木馬のように、敵の戦車に乗り込んで移動する戦略だ。CD8+T細胞は血液脳関門を自由に通過できるため、寄生虫はこれを利用して脳内に侵入する。
なぜ健康な人は発症しないのか
免疫細胞に侵入されたら、もう手の打ちようがないように思える。だが人体には最終防衛ラインがあった。
バージニア大学のタジ・ジャヤティレケ博士らの研究チームは、トキソプラズマに感染したCD8+T細胞を詳しく調べた。すると、感染細胞内でGABPA転写因子が大量に産生されていることが判明した。
GABPAは細胞の遺伝子スイッチを操作するタンパク質だ。このGABPAが特定の遺伝子をONにすると、感染した免疫細胞は自ら死を選ぶ。寄生虫を道連れにした自爆だ。
この仕組みはアポトーシスと呼ばれる。プログラムされた細胞死とも言われ、がん細胞の抑制など体内で重要な役割を果たしている。トキソプラズマ感染でも、同じメカニズムが働いていたのだ。
免疫不全者が危険にさらされる理由
この自爆スイッチが正常に機能するのは、健全な免疫システムがあってこそだ。エイズ患者や臓器移植後の免疫抑制剤使用者では、このメカニズムが十分に働かない。
研究チームがマウス実験で確認したところ、GABPAの働きを抑えると、トキソプラズマ感染による死亡率が劇的に上昇した。感染細胞が自壊できないため、寄生虫が脳内で爆発的に増殖してしまう。
トキソプラズマ脳症と呼ばれる重篤な状態では、脳に膿瘍ができ、痙攣や意識障害を引き起こす。妊娠中の初感染も危険で、胎児に先天性障害を起こすリスクがある。
感染経路と日常生活での予防


猫と暮らす人が知るべきこと
トキソプラズマの最終宿主は猫科動物だ。猫の小腸でのみ有性生殖ができ、オーシストを排出する。つまり猫を飼っている家庭では、感染リスクが高まる可能性がある。
ただし過度な心配は不要だ。室内飼いの猫で、生肉を与えていなければ、感染リスクは極めて低い。むしろ危険なのは野良猫の糞が混じった土や砂場だ。
ガーデニングや畑仕事の後は、必ず手をよく洗う。子どもが砂場で遊んだ後も同様だ。猫のトイレ掃除は、妊娠中の女性は避けたほうがいい。どうしても必要なら、使い捨て手袋とマスクを着用する。
食事から感染するルート
実は、猫よりも食事からの感染のほうが一般的だ。トキソプラズマは豚肉や羊肉、鹿肉などにシスト(嚢胞)として潜んでいる。
フランスやドイツなど生肉文化がある国では、感染率が50%を超える地域もある。日本でも生レバーやユッケを食べる習慣があった時代、感染率は比較的高かった。
予防法は簡単だ。肉は中心部まで75度以上で加熱する。冷凍も有効で、マイナス20度で24時間以上冷凍すれば寄生虫は死滅する。
野菜や果物も注意が必要だ。土壌に混入した猫の糞便由来のオーシストが付着している可能性がある。流水でよく洗い、できれば皮をむく。
世界の感染率の違い
トキソプラズマの感染率は地域によって大きく異なる。フランスでは成人の約55%が抗体陽性だが、韓国では約5%に過ぎない。
この差は食文化と深く関係している。フランスでは生に近い肉料理が好まれ、野良猫も多い。一方、韓国では肉をしっかり火を通して食べる習慣がある。
日本の感染率は約10%と推定されている。数十年前は20%程度だったが、生肉食の減少と衛生環境の向上で低下傾向だ。
新発見がもたらす医療への影響


新薬開発の可能性
バージニア大学の発見は、新しい治療法開発の道を開く。現在のトキソプラズマ治療薬は、休眠状態のシストには効果がない。脳や筋肉に潜んだ寄生虫を完全に排除することは困難だ。
ジャヤティレケ博士は、GABPAの働きを強化する薬剤の開発を提案している。感染細胞の自爆を促進できれば、免疫不全患者でも重症化を防げる可能性がある。
さらに興味深いのは、この発見が他の細胞内寄生体にも応用できる点だ。リーシュマニアやマラリア原虫など、免疫細胞に侵入する病原体は多い。同じメカニズムが働いているなら、幅広い感染症治療に役立つ。
精神疾患との関連性
トキソプラズマ感染と行動変化の関係は、長年議論されてきた。ラットを使った実験では、感染個体が猫を恐れなくなる現象が報告されている。
人間でも、統合失調症や衝動的行動との関連を示唆する疫学研究がある。ただし因果関係は証明されていない。今回の発見により、脳内での寄生虫の挙動がより詳しく解明されれば、この謎にも迫れるかもしれない。
スタンフォード大学の別の研究チームは、トキソプラズマが脳内のドーパミン産生を変化させる可能性を指摘している。今後、神経科学と寄生虫学の境界領域で、新たな発見が期待される。
進化的な軍拡競争
寄生虫と宿主の関係は、何百万年もの進化の産物だ。トキソプラズマが免疫細胞に侵入する能力を獲得すれば、宿主はそれに対抗する自爆メカニズムを進化させる。
この軍拡競争は今も続いている。一部のトキソプラズマ株は、GABPAによる自爆を回避する能力を持つ可能性がある。そうした株が広がれば、新たな公衆衛生上の脅威になるかもしれない。
バージニア大学のチームは、異なる地域由来のトキソプラズマ株で、GABPA応答性に違いがあるか調べている。地域ごとの感染率の差が、寄生虫側の遺伝的多様性と関係している可能性もある。



免疫って、すごく賢いんだね!
そうなんです。何百万年もかけて洗練されてきた防御システムなんですよ
トキソプラズマの研究は、免疫学の新たな一面を明らかにした。敵の侵入を許しても、最終的には道連れにする。この巧妙な仕組みが、私たちの健康を日々守っている。
研究チームは今後、臨床応用に向けた研究を進める予定だ。免疫不全患者を守る新薬の開発には、まだ時間がかかるだろう。だが、この発見は確実に医療の未来を変える一歩となる。
参考文献:
One in three people carry this brain parasite but the body has a kill switch
出典: ScienceDaily
アイキャッチ画像: Photo by Cheng Qi Huang on Unsplash








コメント